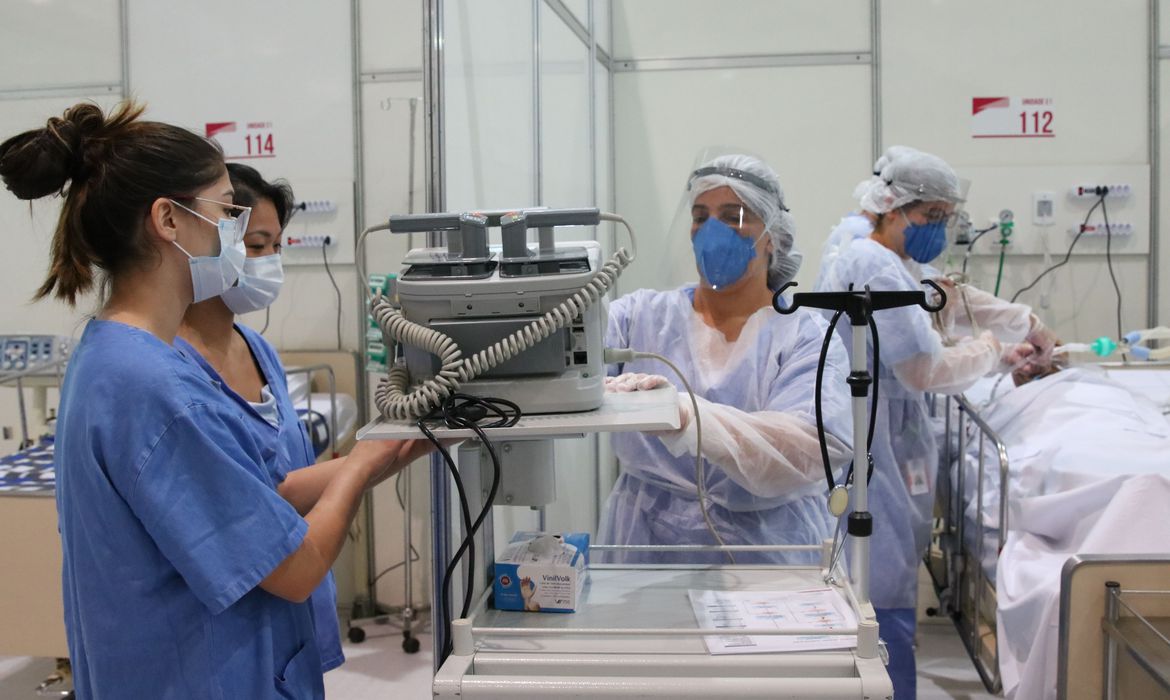
O uso off label de medicamentos em combate da pandemia da Covid-19
10 de abril de 2020, 18h01
Quando o tratamento indicado para a cura ou o controle eficaz de uma doença não se achem resguardados em prescrições ou protocolos médicos e os meios convencionais disponíveis em procedimentos, terapêuticas e medicamentos silenciam a resposta de êxito adequada, o uso off label de medicamentos desafia atualmente a medicina, precisamente nos planos bioético e jurídico.
Neste cenário, presente a discussão atual do uso da cloroquina ou da hidroxicloroquina, associada à azitromicina, no tratamento da Covid-19, sem estudos científicos conclusivos para a validação de sua eficácia e sem consenso médico (1). No entanto, à falta do medicamento certo, pessoas continuam morrendo e mais pessoas morrem em conta assustadora e trágica de vidas não salvas. A chamada “situação limítrofe" ou o “dilema do paraquedas” (2).
Não há negar os esforços médicos para as práticas de tratamento medicamentoso fora de bula, em busca da chance de uma cura por meio de prescrições médicas atípicas. Eles harmonizam a demanda atual de saber a saúde e o direito à vida como supradireitos fundamentais de todas as pessoas. Nessa diretiva, o diálogo de fontes torna-se urgente entre direito e medicina, no enfrentamento da pandemia da Covid-19.
Anota-se, de logo, na expressão do ministro Luís Felipe Salomão que o off label corresponde ao uso “essencialmente correto de medicação aprovada em ensaios clínicos e produzida sob controle estatal, apenas ainda não aprovado para determinada terapêutica” (3).
Por tal diretiva, consoante a Declaração de Helsinque II, “no tratamento da pessoa doente, o médico deve ter liberdade para usar uma nova medida diagnóstica ou terapêutica se, em seu julgamento, esta oferecer esperança de salvar a vida, restabelecer a saúde ou aliviar o sofrimento”. O Código de Ética Médica (artigo 32), exalta que o médico deve usar todos os meios disponíveis de tratamento a seu alcance, em favor do paciente. Eis, a questão posta.
Assente que os fármacos off label tem percentuais elevados de vendas em farmácias ou de uso nos hospitais, torna-se inequívoco tratar-se de uma prática necessária em alguns casos e que interage com a liberdade de escolha dos médicos nesse tipo de prescrição.
A liberdade terapêutica constitui princípio fundamental da prática médica (4) lecionando Carla Barbosa e Mafalda Francisco Matos, juristas portuguesas: “a prescrição off label tem, seu fundamento, precisamente, nessa faculdade do médico”, importando que a esta liberdade terapêutica liga-se, neste sentido, a liberdade de prescrição.
Expressam, com precisão cirúrgica: “O médico é livre de prescrever aquele que considera ser o melhor tratamento para a saúde do seu paciente, para o melhor benefício do mesmo e é, pois, nesta medida que se justifica que exista uma prescrição como a que é feita a título off label. Esta prescrição deve ser feita de forma livre e serena, não se encontrando motivada por influências e vicissitudes estranhas à saúde daquele paciente concreto”. (5)
De fato. Contribuição significativa tem dado o Superior Tribunal de Justiça em desate da questão: “o entendimento firmado por esta Corte Superior é no sentido de que o plano de saúde pode limitar a cobertura de determinadas doenças, mas não o tipo de terapêutica indicada por profissional habilitado na busca da cura, ainda que se trate de medicamento para uso off label”. (STJ – Ag. em REsp. 1.504.531 – RJ (2019/0139258-3), Rel. Min. Paulo de Tarso Sanseverino, j. em 27 de março de 2020, DPJ de 7.4.2020).
A seu turno, asseverou o ministro Ricardo Villas Bôas Cueva, em recente julgamento (16.3.2020): “no caso concreto não se trata de medicamento não registrado na Anvisa e sim de uso off label do medicamento (..) Cabe ressaltar que, havendo cobertura para a moléstia cujo tratamento depende do uso da medicação pleiteada, não pode a requerida afastar a prescrição do médico que acompanha o autor que, na qualidade de profissional, detém o conhecimento e a técnica para avaliar corretamente a necessidade do tratamento em questão.”(6)
Odioso e inaceitável prejuízo à vida do paciente enfermo será negar-lhe medicamento off-label, quando medicamentos convencionais não lhe socorram ao processo de cura.
Recolhe-se a ponderação: “ainda que não tenha uma definição uniforme, o CFM entendeu que o uso off label ocorreria por indicação médica pontual e específica, sob o risco do profissional que o indicou” (REsp. 1.729.566). Assim, cumprirá ao médico assinalar motivadamente em prontuário a opção ou a necessidade extrema do uso, legitimando a conduta, para além de dispor do consentimento informado do paciente (pessoal ou por diretivas de testamento vital).
Irrecusável a distinção entre a prescrição off label e o manejo experimental de medicamentos, sob pena de a prescrição imbricar-se em uma área experimental, desnaturando-se.
A diferenciação é feita por C. Barbosa e Mafalda Matos destacando que “na prescrição off label, assiste-se a uma efectiva intervenção terapêutica, a uma intenção de debelar a doença que aquele doente, em concreto, apresenta”. Mais precisamente: “se a prescrição é feita para obter um benefício directo para aquele paciente concreto, procurando uma efectiva melhoria da sua saúde e bem-estar, motivada tão só pelo interesse do doente, aí já entramos no campo terapêutico e estaremos em sede de um uso off label do medicamento.” (7)
Colocadas estas observações, questiona-se:
(i) Em não havendo comprovação cientifica, como deve ser tratada a prescrição de medicamentos sem a devida formulação em bula?
O problema não é recente. Em 2001 ocorreram 150 milhões de usos off label de medicamentos para pacientes ambulatoriais nos E, o que correspondeu a 21% do uso total; implicando, dois anos depois, o incremento de 80% das vendas de medicamentos para usos não aprovados.
Daí, a Avisa publicizou que cada medicamento registrado no Brasil recebe a aprovação da agência para uma ou mais indicações e uma vez este comercializado, o seu uso off label é feito por conta e risco do médico que o prescreve” (23.5.2005).
Aliás, o Conselho Federal de Medicina, pelo Parecer 13/2004, de 14 de abril, ditou que esta prescrição será considerada como pesquisa médica combinada com cuidados profissionais. E pronunciou no sentido de o uso de material/medicamento off label não poder ser tratado de forma ampla e geral, devendo ser analisado casuisticamente” e “não ser cabível a edição de uma norma geral pelo Conselho, porque estar-se-ia a disciplinar de forma genérica situações que são específicas e casuísticas, as vezes até mesmo sem comprovação cientifica” (Parecer 482/2013, de 19 de novembro).
Ao depois, definiu que o uso off label de medicamentos é de responsabilidade do médico, devendo arcar ética, criminal e civilmente pelas consequências de suas ações, já que ciente de que a utilização do fármaco é indicada para outras finalidades” (Parecer de 537/2015, de 21 de outubro).
Lado outro, o artigo 7º da Lei 12.842/2013, de 10 de julho (Lei do Ato Médico), dispõe que “compreende-se entre as competências do Conselho Federal de Medicina editar normas para definir o caráter experimental de procedimentos em Medicina, autorizando ou vedando a sua prática pelos médicos”.
Antes disso, a Resolução CFM 1.982/2012, de 20 de janeiro, adotou normas éticas para o reconhecimento de novos procedimentos/terapias médicas pelo Conselho Federal de Medicina.
Em outro giro, no Parecer de 02/2016-CFM, de 20.1.2016, observou-se que “Os procedimentos médicos off label são aqueles em que se utilizam materiais ou fármacos fora das indicações em bula ou protocolos, e sua indicação e prescrição são de responsabilidade do médico. Não compete às Comissões de Ética emitir juízo de valor sobre o uso de off label.”
(ii) Diante do entendimento de constituir o uso off label de medicamentos como pesquisa médica (CFM-Proc.-Consulta 2.437/2003), justamente à falta de indicações terapêuticas especificas, como se explica ausente normas que disciplinem o tratamento experimental?
Impõem-se urgentes normativos do caráter experimental dos procedimentos médicos, sobretudo quando os novos procedimentos, podem ser aprovados pelo CFM (Res.-CFM 1.982/2012).
Enquanto isso a proteção do paciente pelo direito, no binômio justiça e medicina, serve a reconhecer a importância de novos procedimentos médicos terapêuticos, justificando a evolução da jurisprudência dos tribunais em construção dialogada com o progresso da medicina.
Julgamento paradigma ocorreu no REsp. 1.279.241 (Rel. p/Acórdão Min. Raul Araújo; j. em 2.10.2014) decidindo o STJ que em situações onde os tratamentos convencionais não forem suficientes ou eficientes, e em existindo tratamento experimental, idôneo porque sediado em instituição de reputação cientifica reconhecida, este tratamento passará a ser o único de real interesse para o contratante segurado, configurando o tratamento mínimo garantido pelo artigo 12 da Lei 9.656/1998.
Ou seja, o entendimento de que "os planos de saúde podem, por expressa disposição contratual, restringir as enfermidades a serem cobertas, mas não podem limitar os tratamentos a serem realizados, inclusive os medicamentos experimentais." (STJ – 4ª Turma, Ag. Reg, no Agravo em REsp. 2015/0173692-6, Rel. Min. Maria Isabel Galotti, j. em 15.9.2015).
Indiscutível que os benefícios potenciais de novos medicamentos em usos off label ou de procedimentos médicos experimentais devem ser sopesados em relação às vantagens dos terapêuticos atuais.
Decisão significativa ofereceu o STJ (RESp 668.216, Rel. Min. Menezes Direito, 15.3.2007): “1. A abusividade da cláusula reside exatamente nesse preciso aspecto, qual seja, não pode o paciente, em razão de cláusula limitativa, ser impedido de receber tratamento com o método mais moderno disponível no momento em que instalada a doença coberta. (…) –
É irrecusável que muitas substâncias concorrem ao uso off label de medicamentos, com extraordinário percentual de manejo para determinados pacientes.
Exemplificam-se: (i) A quetiapina, indicada para o tratamento de doenças mentais, empregada como um agente de acréscimo ao controle do Alzheimer; (ii) o uso off label de sofosbuvir, em suspeita de febre amarela, ocorre por uma indicação médica pontual, específica e excepcional em desconformidade com a bula e sob risco e responsabilidade do profissional que a indicou” (Parecer CRM-MG n. 160/2018); (iii) o emprego de remédios off-label designadamente para o combate à obesidade com uso de diversas substâncias (algumas delas destinadas a diabéticos) como indicações ao emagrecimento; (iv) em outra latitude, o canabidiol, substância encontrada na maconha, cujo uso tem sido útil ao tratamento de determinadas doenças neurológicas, (CFM-Res. 2.113, de 30.12.2014).
De boa nota referir a liberação pela Lei 13.454, de 23.06.2017, da produção, comercialização e consumo, por prescrição médica, de medicamentos aneroxígenos, derivados das anfetaminas, com as substâncias anfepramona, frenpoporex e mazindrol, inibidoras do apetite, proibidas desde 2011 pela Anvisa. A opção terapêutica sofria questionamentos. Aquela autorização legislativa põe mais relevo jurídico ao tema de hoje.
Essas tomadas de decisão são emanadas de uma ética subjacente à ampla defesa do paciente no emprego de medicamentos off label; e formam, a cada passo, a medicina do futuro, para a melhor dignidade do paciente na busca incontida de sua salvação.
Mas não é só: quando a vida humana precisa sobreviver à atual pandemia e cada uma vida equivale à toda humanidade, despedaçada a cada uma de suas perdas de vidas, a solução de uso de medicamentos off label para além de prescrição médica torna-se prescrição ética, como uma outra esperança que se renova. Hallelujah.
Notas
(1) Apesar do dissenso, o Conselho Regional de Medicina do Amazonas recomendou (08.04.20), que o médico adote o tratamento observado o caso (Recom. 101/20) e estudo francês, no International Journal of Antimicrobial Agents, indica evidências de a combinação da hidroxicloroquina com o antibiótico azitromicina poder ser, “especialmente, eficaz no tratamento da doença, reduzindo o tempo de vida do vírus”. (Web: https://www.mediterranee-infection.com/wp-content/uploads/2020/03/Hydroxychloroquine_final_DOI_IJAA.pdf Acesso em 09.04.2020). A HCQ já mostrou eficácia in vitro para o SARS-CoV (coronavírus responsável por uma epidemia na Ásia em 2003).
(2) O “dilema do paraquedas” situa-se, ilustrativamente, na opção de poder usar um paraquedas aparentemente inservível, ao invés de pular no vazio, sem paraquedas algum. A questão foi tratada em artigo no British Medical Journal, onde, com ironia inglesa, define-se o problema (“o paraquedas é útil ou não?). A saber do número de mortes e lesões graves nos “paraquedados” comparados aos “não paraquedados” em quedas definitivamente muito altas, o artigo considerou necessário um estudo para que o uso do paraquedas possa ser dito “baseado em evidências” (!).
Web: http://apps.einstein.br/revista/arquivos/PDF/1522-EC_V8_N4_p188-9.pdf Acesso em 09.04.2020).
(3) STJ – 4ª Turma – REsp. 1729566, j. em 04.10.2018, DJe de 30.10.2018, Rel. Min. Luís Felipe Salomão. “7. A prescrição de medicamento para uso off-label não encontra vedação legal (…)”
(4) Afirma E. Di Paolo, que a liberdade terapêutica encontra-se, desde logo, plasmada no próprio Código Deontológico dos Médicos, quando se confere a estes profissionais independência, autonomia, isenção e liberdade nas suas escolhas terapêuticas, nas suas prescrições, de acordo com a ciência e a sua consciência (in Di Paolo, E., et al., “Unlicensed and off-label drug use in a Swiss paediatric university hospital”, Swiss Medical Weekly, n.º 136, 2006).
(5) BARBOSA, Carla. MATOS, Mafalda Francisco. Prescrição off-label, direito à informação, consentimento informado e processo clínico eletrônico no direito português. Revista Cadernos Ibero-Americanos de Direito Sanitário. 2016 jul./set, 5(3):157-179; p. 166.
(6) AgInt. no Ag. em REsp. 1429511- SP (2019/0012561-7, j. em 16.03.2020;
(7) Idem. BARBOSA, Carla. MATOS, Mafalda Francisco p. 164;
Referências bibliográficas:
BARBOSA, Carla. MATOS, Mafalda Francisco. Prescrição off-label, direito à informação, consentimento informado e processo clínico eletrônico no direito português. Revista Cadernos Ibero-Americanos de Direito Sanitário. 2016 jul./set, 5(3):157-179;
RAMOS, Karina Alves. O uso off label de medicamentos e a busca por evidências orientadoras de conduta: uma abordagem necessária. Web: http://www.cpgls.pucgoias.edu.br/7mostra/Artigos/SAUDE%20E%20BIOLOGICAS/O%20uso%20off%20label%20de%20medicamentos%20e%20a%20busca%20por%20evidencias%20orientadoras%20de%20conduta.pdf Acesso em 09.04.2020
Encontrou um erro? Avise nossa equipe!